
題目列表(包括答案和解析)
 運用化學反應原理研究元素及其化合物的反應對生產、生活有重要意義.
運用化學反應原理研究元素及其化合物的反應對生產、生活有重要意義. (2012?淄博一模)硫及其化合物在國民生產中占有重要的地位.
(2012?淄博一模)硫及其化合物在國民生產中占有重要的地位.| 1 | 2 |
| 時間(S)濃度 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(A)mol?L-1 | 0.100 | 0.070 | 0.050 | c3 | a | b |
| c(B)mol?L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |

| 16 |
| 3 |
| 16 |
| 3 |
 CH3CH2OH(g)+3H2O(g) 25℃時,K=2.95×1011
CH3CH2OH(g)+3H2O(g) 25℃時,K=2.95×1011 |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
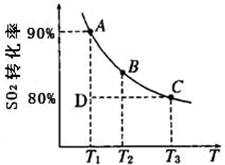 硫及其化合物在國民生產中占有重要的地位.
硫及其化合物在國民生產中占有重要的地位.| 1 | 2 |
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com