
題目列表(包括答案和解析)
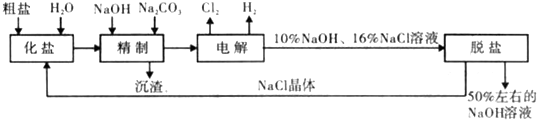
2- 4 |

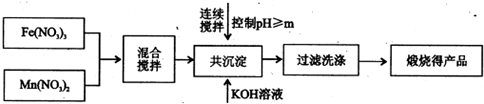
| 開始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
| ||
| x |
| 2 |
| 1 |
| 2 |
| a+b |
| x |
| 1 |
| 2 |
| a+b |
| x |
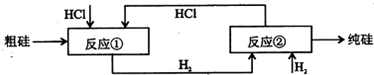
| ||
| ||
 Ca3(P04)2+5Fe
Ca3(P04)2+5Fe Ca3(P04)2+5Fe
Ca3(P04)2+5Fe
| ||
| ||
| 沸騰爐溫度/℃ | 600 | 620 | 640 | 660 |
| 爐渣中CuSO4的質(zhì)量分數(shù)/% | 9.3 | 9.2 | 9.0 | 8.4 |
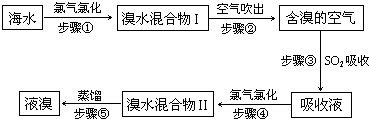
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com