
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | ������ӵ����ʽ��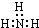 | B�� | S2-�ĽY(ji��)��ʾ��D�� | ||
| C�� | CH4�����ģ��ʾ��D�飺 | D�� | �����ʽ��ʾHCl�γ��^�̣� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
| ���W�I | H-H | N-H | N��N |
| �I��/kJ•mol-1 | 436 | 391 | 945 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | 늽��^����ꎘO�]�К��w���� | |
| B�� | 늽��^�����D(zhu��n)�Ƶ���ӵ����|(zh��)������0.4 mol | |
| C�� | ԭCuSO4��Һ�ĝ�Ȟ�0.1 mol•L-1 | |
| D�� | 늽��^����ꖘO�ռ����Ě��w�w�e��2.24 L���˛r�£� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
| A�� | CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=890.3 kJ•mol-1 | |
| B�� | CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890.3 kJ•mol-1 | |
| C�� | CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3 kJ•mol-1 | |
| D�� | 2H2��g��+O2��g���T2H2O��l����H=-571.6 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �����ᷴ�� | B�� | �Ƿşᷴ�� | ||
| C�� | ���pС�ķ��� | D�� | ������Ч����������Ч�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �ڢޢߢ� | B�� | �٢ܢ�� | C�� | �ۢݢߢ� | D�� | �ۢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | v��H2��=0.3 mol•L-1•min-1 | B�� | v��N2��=0.05 mol•L-1•s-1 | ||
| C�� | v��N2��=0.2 mol•L-1•min-1 | D�� | v��NH3��=0.3 mol•L-1•min-1 |
�鿴�𰸺ͽ���>>
���H�WУ��(y��u)�x - �������б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com